服务中心
CUSTOMER SERVICE
钛及其合金因其优异的机械性能、生物相容性和耐腐蚀性,被广泛应用于骨科植入物。然而,钛植入物表面因生物惰性而导致的细菌感染和骨整合延迟问题,一直是临床上的两大挑战。细菌感染不仅会导致手术失败,还可能引发严重的并发症,甚至危及患者生命。而骨整合延迟则可能导致植入物松动,进一步加剧感染风险。如何同时解决这两个问题,成为了当前研究的热点。
最近,来自华南理工大学的研究团队在《Biomaterials》期刊上发表了一项突破性研究,他们开发了一种基于介孔二氧化硅纳米颗粒(MSNs)的功能化钛植入物,能够实现抗菌肽(AMP)的可控释放,显著提升了植入物的抗菌性能和骨整合能力。这一研究成果为骨科植入物的未来发展提供了新的思路。

研究团队通过将抗菌肽HHG36负载到二硒键桥接的介孔二氧化硅纳米颗粒(MSNs)中,并将其固定在钛植入物表面,制备出了一种新型功能化钛植入物(Ti-M@A)(见Fig.1a)。这种植入物不仅能够持续释放抗菌肽,有效杀灭多种临床常见细菌(如金黄色葡萄球菌、大肠杆菌、铜绿假单胞菌和耐甲氧西林金黄色葡萄球菌),还能通过硒元素促进骨髓间充质干细胞的成骨分化,显著提升骨整合效果。
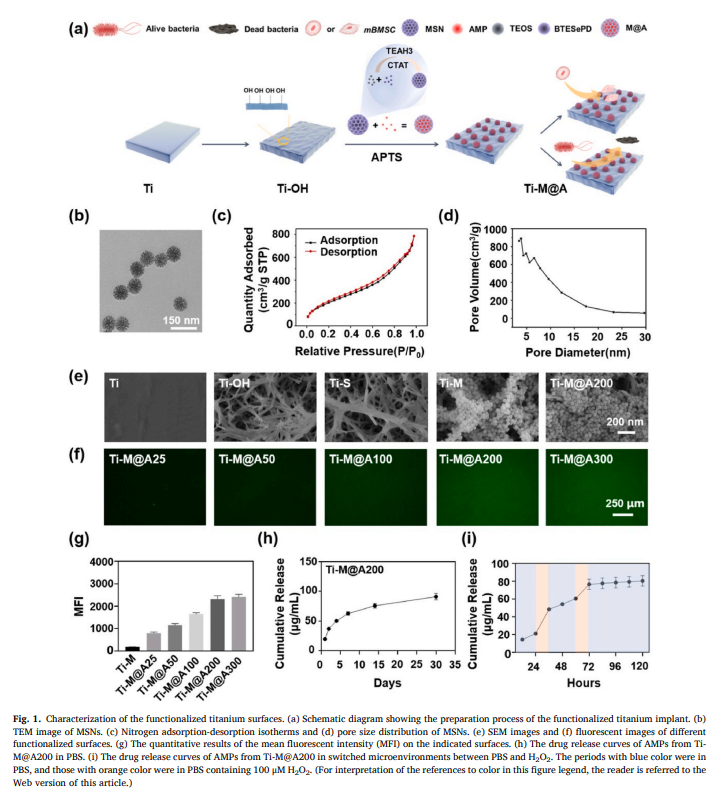
可控释放:响应细菌感染的微环境
该植入物能够在生理条件下持续释放抗菌肽长达30天,且在细菌感染引发的氧化应激微环境中(如过氧化氢浓度升高时),抗菌肽的释放速度会显著加快,实现“按需释放”。这种智能响应机制确保了抗菌肽在感染发生时能够迅速发挥作用,而在正常生理条件下则保持低毒性。
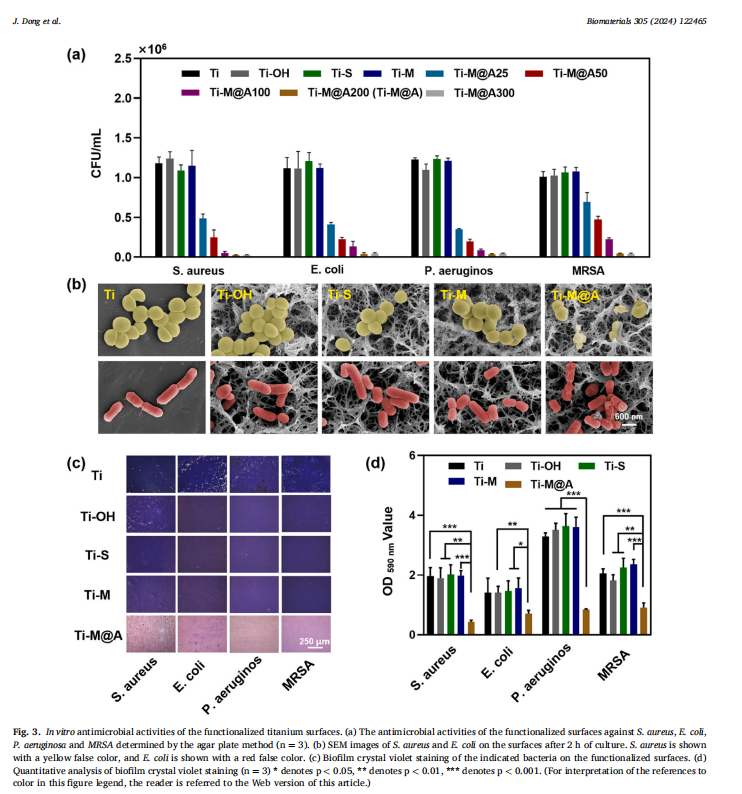
优异的生物相容性与抗炎效果
体外实验表明,Ti-M@A植入物对骨髓间充质干细胞和巨噬细胞均表现出良好的生物相容性。此外,植入物表面的硒元素能够有效清除巨噬细胞中的活性氧(ROS),促进巨噬细胞向抗炎的M2型极化从而减轻炎症反应,促进组织修复。(见Fig.5)

为了评估巨噬细胞的极化,采用流式细胞术检测不同底物上M1型巨噬细胞(CD86)和M2型巨噬细胞(CD206)的特征性标记物。巨噬细胞(RAW 264.7)被移入24孔板中,用PBS冲洗。然后用细胞刮板收集细胞,用封闭缓冲液冲洗20 min,然后清洗细胞并染色CD11b/BV510 、CD86/APC、CD206/FITC,利用流式细胞仪精确地量化这些标志物的表达,进行极化分析。
(流式细胞分析数据来自北京层浪生物技术有限公司,FongCyte™)
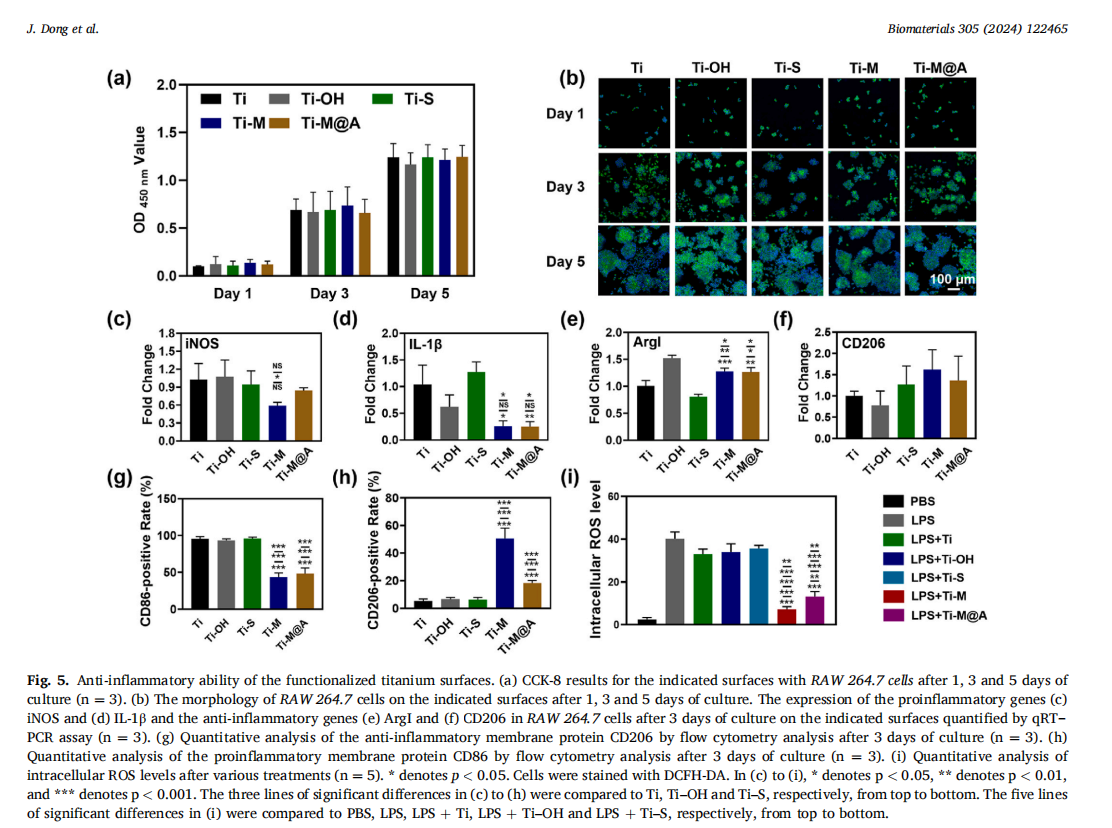
优异的生物相容性与抗炎效果
在兔子的骨缺损模型中(见Fig.6),Ti-M@A植入物在感染和非感染条件下均表现出优异的骨整合能力。特别是在感染模型中(见Fig.7),Ti-M@A能够杀灭超过98.82%的金黄色葡萄球菌,并显著减少炎症细胞的浸润,促进骨组织的再生。
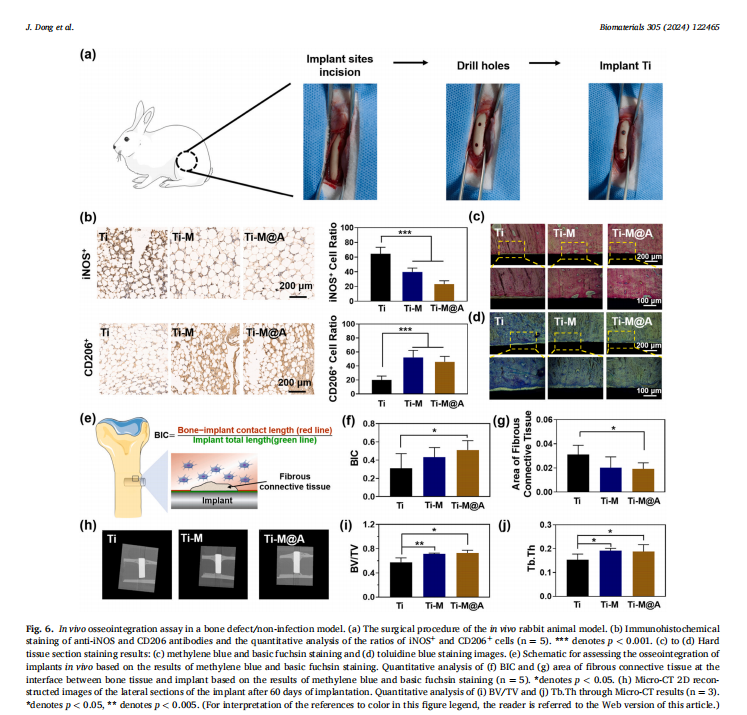

这项研究不仅提供了一种新型的功能化钛植入物设计策略,还展示了如何通过纳米材料的智能响应机制,实现抗菌与骨整合的双重功能。Ti-M@A植入物的成功开发,为未来骨科植入物的临床应用提供了新的可能性,尤其是在预防植入物相关感染和促进骨整合方面具有重要的临床意义。此外,研究团队还展示了该系统的广泛适用性,通过替换不同的抗菌肽(如YGFGG),可以进一步扩展其应用范围。未来,这种基于MSNs的功能化钛植入物有望在更多临床场景中得到应用,为患者提供更安全、更有效的治疗方案。
随着生物材料科学的不断进步,功能化植入物的研究正朝着更加智能化、个性化的方向发展。这项研究的成功,不仅为骨科植入物的设计提供了新的思路,也为其他领域的生物材料研究带来了启发。我们期待在未来层浪生物能助力更多类似的创新成果,为患者带来更好的治疗效果。
参考文献:
Dong, J., Chen, F., Yao, Y., et al. (2024). Bioactive mesoporous silica nanoparticle-functionalized titanium implants with controllable antimicrobial peptide release potentiate the regulation of inflammation and osseointegration. *Biomaterials*, 305, 122465.